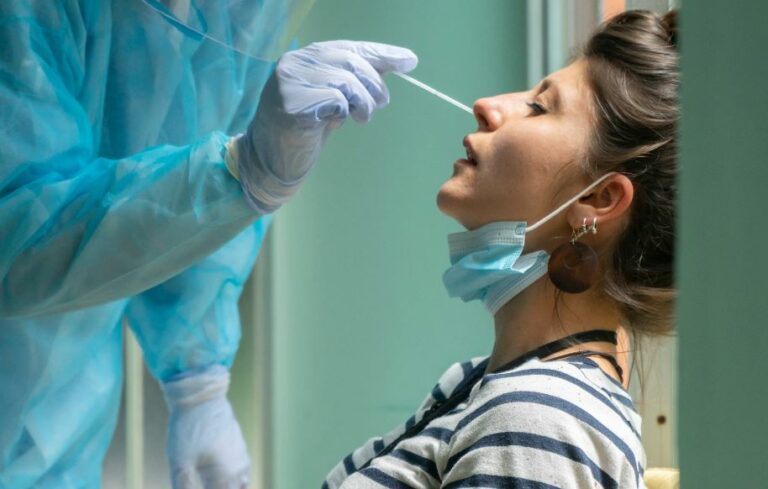
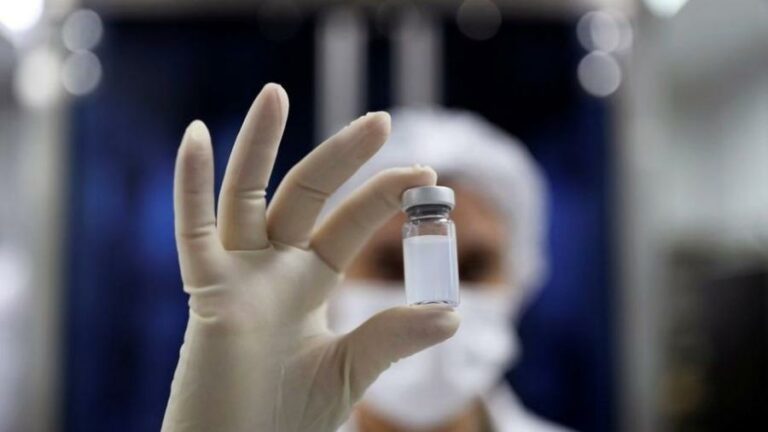
Última etapa do maior estudo epidemiológico sobre a Covid-19 é realizada no Brasil
Foi iniciada, no dia 25 de janeiro, a etapa final do maior estudo epidemiológico sobre Covid-19 realizado no Brasil. O EPICOVID-19 BR 2: Inquérito Nacional de Soroprevalência de Acesso Expandido vai concluir os níveis de infecção da população a partir do levantamento em 133 municípios no país. Nesta fase, que acontece em um momento estratégico…